Лечение климакса при раке молочной железы
Содержание статьи
Коррекция климактерических расстройств у больных раком молочной железы: актуальные методы и перспективы
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России, Москва, Россия
Коррекция климактерических расстройств у больных раком молочной железы (РМЖ) является методом поддержания не только качества жизни, но и ее продолжительности, в том числе за счет снижения частоты отказа от противорецидивной терапии. Самым эффективным методом лечения остается менопаузальная гормонотерапия (МГТ), которая, за некоторыми исключениями, противопоказана при РМЖ. Фитоэстрогены и ингибиторы обратного захвата серотонина (и норадреналина) являются альтернативой для купирования вазомоторных симптомов (ВМС). При отсутствии эффекта от негормональных методов лечения генитоуринарного менопаузального синдрома (ГУМПС) следует решать вопрос о терапии вагинальными эстрогенами. К перспективным направлениям относятся использование тканеселективного эстрогенового комплекса, эстетрола, оспемифена и вагинального дегидроэпиандростерона. Снижение минеральной плотности кости и переломы у больных РМЖ являются следствием целого ряда причин. К эффективным методам лечения относятся бисфосфонаты и деносумаб.
Качество жизни пациенток, больных раком молочной железы (РМЖ), остается нерешенной клинической задачей. И перед врачами во всем мире становится эндокринная дилемма: необходимо одновременно блокировать эффекты эстрогенов для снижения риска рецидивов РМЖ и купировать проявления дефицита эстрогенов (климактерического синдрома) для поддержания качества жизни больных [1].
За последние 40 лет наблюдается улучшение в частоте выживаемости после постановки диагноза РМЖ. Однако большинство женщин имеют низкое качество жизни, связанное с тяжелыми приливами жара, бессонницей, сухостью во влагалище, диспареунией, остеопорозом и другими проявлениями климактерического синдрома [2].
Число женщин, перенесших РМЖ в анамнезе, постоянно повышается, поэтому климактерические расстройства в указанной группе становятся крайне важной проблемой с коротко- и долгосрочными последствиями для здоровья и качества жизни (табл. 1) [3].
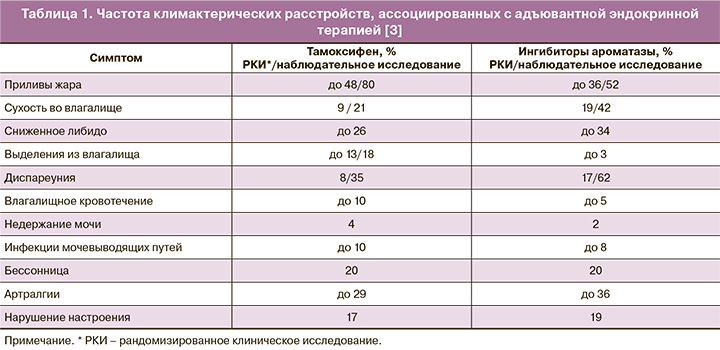
Около 80% женщин, получающих терапию тамоксифеном, имеют вазомоторные симптомы (ВМС), при дополнительной овариальной супрессии приливы развиваются у 93% женщин [4].
Полагают, что интенсивность приливов жара у пациенток, больных РМЖ, выше, чем у женщин с естественной менопаузой. Приливы жара на фоне терапии тамоксифеном обычно более тяжелые по сравнению с терапией ингибиторами ароматазы (ИА) [3]. У молодых пациенток с индуцированной менопаузой климактерические симптомы более тяжелые, чем у женщин в постменопаузе.
Климактерические расстройства у женщин, больных РМЖ, могут быть связаны: с естественной менопаузой, возникшей параллельно с диагнозом РМЖ; возобновлением симптомов после отмены менопаузальной гормонотерапии (МГТ) в случае постановки диагноза РМЖ; риск-редуцирующей билатеральной аднексэктомией; химиотерапией или супрессией функции яичников агонистами гонадотропин-рилизинг-гормона (аГнРГ) в пременопаузе; адъювантной терапией тамоксифеном или ИА [5].
Выявлено, что тяжелые приливы жара могут приводить к отказу от лечения антиэстрогенами [6]. Как следствие, по данным зарубежных авторов, до 28% женщин, больных РМЖ, не привержены адъювантной терапии, 34% отмечают, что врачами не задавался вопрос о приливах жара и ночной потливости, и только 25% женщин было рекомендовано лечение [7]. Полученные данные указывают на возможное повышение риска рецидивов РМЖ за счет низкого качества жизни на фоне терапии заболевания и, как следствие, отказа от нее.
Коррекция вазомоторных симптомов у больных раком молочной железы
Известно, что МГТ может купировать до 90% приливов, однако вызывают обеспокоенность системное воздействие эстрогенов и возможное повышение частоты рецидивов у женщин, перенесших РМЖ, что крайне ограничивает ее использование [8].
За последние 20 лет проведено множество исследований, направленных на поиск эффективных не-эстрогенсодержащих методов лечения для женщин, перенесших РМЖ [2].
Фитоэстрогены похожи на 17β-эстрадиол по химической структуре [9] и могут обладать эстрогенным и антиэстрогенным эффектом. Результаты исследований влияния их на прогноз у больных РМЖ неоднозначны. Большинство данных поддерживают представления о безопасности их использования, некоторые даже указывают на снижение риска рецидивов и смертности на фоне их приема [3].
Согласно данным исследования на клеточной линии РМЖ, экстракт цимицифуги блокировал рост, особенно при повышенной экспрессии HER2 [9, 10]. Согласно данным систематического обзора 26 статей, не выявлено взаимосвязи между приемом цимицифуги и повышением риска РМЖ [11].
Однако, согласно данным метаанализа 16 исследований, не выявлено различий между цимицифугой и плацебо в частоте и тяжести приливов [12]. Эффективность фитоэстрогенов при РМЖ не была доказана в рандомизированных клинических исследованиях [3]. В целом эффект плацебо может достигать 50% у данной группы женщин [13].
Таким образом, не выявлено значительной эффективности влияния цимицифуги на приливы жара у больных РМЖ, а также негативного влияния на риск РМЖ [11].
Альтернативные методы
Норадреналин и серотонин являются важными нейротрансмиттерами, влияющими на терморегуляцию, и участвуют в патогенезе приливов жара. Эстрогены влияют на их высвобождение и на количество их рецепторов.
Ингибиторы обратного захвата серотонина (и норадреналина) одинаково эффективны у женщин, перенесших РМЖ, независимо от приема тамоксифена или ИА (несмотря на то, что на фоне приема тамоксифена приливов обычно больше) [14].
Однако некоторые из них (пароксетин, флуоксетин, сертралин) способны ингибировать цитохром Р450 2D (CYP2D6), метаболизирующий тамоксифен в его активную форму – эндоксифен [4]. Оптимальным вариантом является выявление показаний и подбор препарата совместно с неврологом/психиатром. Ниже представлены основные препараты, благоприятно воздействующие на ВМС у женщин (табл. 2).
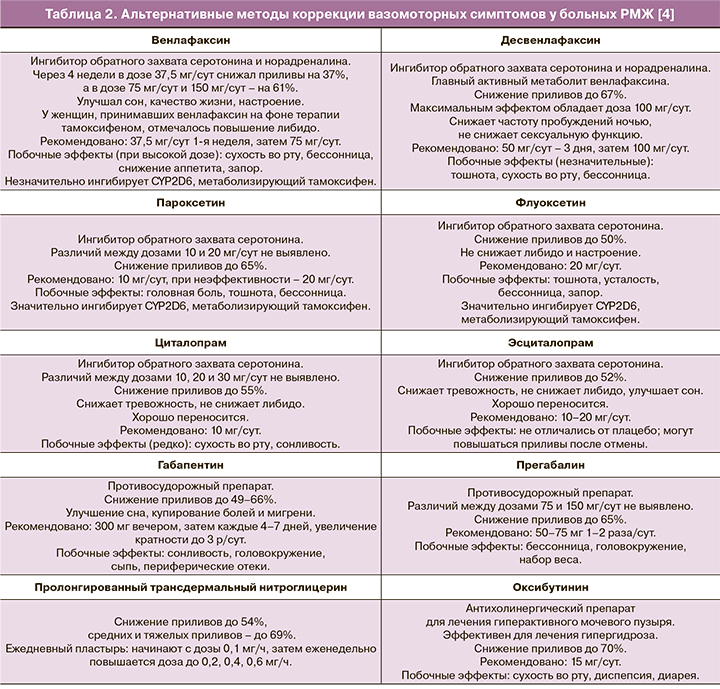
Иглоукалывание, когнитивная поведенческая терапия и некото…
Сметник А.А., Родионов В.В., Кометова В.В.
Источник
Менопауза и рак молочной железы
Менопауза сама по себе не ассоциируется с увеличенным риском развития рака. Однако, как бы там ни было, раковые заболевания, включая рак молочной железы, прогрессируют с возрастом. К тому же, некоторые лекарственные препараты, принимаемые для облегчения симптоматики климактерического периода, могут увеличить или уменьшить риск развития рака.
Какие факторы риска заболевания раком молочной железы?
Некоторые факторы увеличивают риск развития рака молочной железы. Однако, наличие многих факторов риска не обозначает, что у женщины разовьется рак молочной железы, и наоборот, отсутствие факторов риска не обозначает, что он у нее не разовьется.
Возраст — единственный самый важный фактор развития рака молочной железы. Шансы развития болезни увеличиваются с возрастом. Среди женщин с диагнозом рак молочной железы примерно 70% старше 50 лет, и почти половина находится в возрасте 65 лет и старше. Личный риск выше, если непосредственный член вашей семьи (мама, сестра или дочь) болел раком молочной железы, особенно, если это заболевание протекало в раннем возрасте. Также, у женщин, прошедших биопсию молочной железы (забор образцов ткани груди), результаты которой свидетельствовали о начале болезни, например, астенической гиперплазии, вероятность заболеть раком молочной железы выше.
К другим факторам риска относятся:
Рак в одной из молочных желез (может повториться или развиться в другой груди)
Поздняя менопауза (после 55 лет)
Ранняя менструация (раньше 12 лет)
Рождение первого ребенка после 30 лет
Отсутствие детей
Увеличивает ли заместительная гормональная терапия (ЗГТ) риск рака молочной железы?
Наглядные примеры наводят на мысль, что чем дольше женский организм поддерживается женскими гормонами (выработанными телом, принимаемыми в виде медикаментов или пластыря), тем больше вероятность развития рака молочной железы.
Заместительную гормональную терапию можно назначать в постклимактерический период женщинам с симптомами менопаузы. Чем дольше женщина принимает ЗГТ, тем выше шансы обнаружения у нее рака молочной железы.
Можно ли предотвратить рак молочной железы?
Несмотря на то, что действенные способы предотвращения рака молочной железы еще не установлены, существуют определенные мероприятия, которые позволяют диагностировать заболевание на ранней ступени его развития, и увеличивают ваши шансы побороть болезнь:
Базовое обследование — прохождение маммограммы — в возрасте 35-40 лет.
Если вам больше 40 лет, делайте маммограмму каждый год или через год (ваш врач может посоветовать вам начать раньше 40 лет, в зависимости от ваших индивидуальных факторов риска).
Проходите обследование груди минимум один раз в год.
Проводите самостоятельное обследование груди каждый месяц.
Каждый день занимайтесь физическими упражнениями, избегайте чрезмерного употребления алкоголя, употребляйте ежедневно необходимое количество солей фолиевой кислоты (0.4 mg) и витамина D (400-800 IU).
Как диагностируется рак молочной железы?
Обнаружение рака молочной железы на ранней стадии — до распространения заболевания за пределы груди — может значительно увеличить шансы эффективности лечения. Коэффициент выживаемости при раке молочной железы увеличивается при обнаружении и лечении заболевания на ранней стадии.
Существует два метода ранней диагностики, которые включают в себя физикальное обследование груди: самостоятельное обследование груди и клиническое обследование груди.
Американское раковое Общество рекомендует женщинам в возрасте 20 лет и старше проводить самостоятельное обследование груди каждый месяц. При правильном проведении обследования женщина привыкает к ощупыванию своей груди и может легко заметить изменения. О любых изменениях необходимо немедленно сообщить врачу.
Женщинам в возрасте 20-39 лет следует проходить осмотр груди у врача каждые три года, а по достижению 40 лет — один раз в год.
Маммография — важный метод ранней диагностики, при котором с помощью малой дозы рентгеновского облучения делается снимок ткани молочной железы. Цель маммограммы — найти отклонения, которые слишком, чтобы их можно было увидеть или ощутить. Однако, с помощью маммограммы определяются не все виды рака молочной железы, вот почему очень важно физикальное обследование груди.
Для того, чтобы определить есть ли у вас повышенный риск рака молочной железы, проконсультируйтесь с вашим врачом.
Источник
Гормонотерапия при раке молочной железы
Гормонотерапия при раке молочной железы сегодня проводится теми же препаратами, что и 20 лет назад, не изменились и основополагающие принципы её назначения, существенное отличие современного подхода в более точном подборе лекарственного средства с ориентировкой на биологические характеристики опухоли и индивидуальные эндокринные показатели пациентки.
Что такое гормонотерапия?
Гормонотерапия при раке молочной железы предполагает применение в лечебных или профилактических целях похожих на половые гормоны лекарственных средств для «обмана» раковой клетки или полное прекращение воспроизводства эндокринных субстанций яичниками, а также синтеза гормонов в жировой ткани.
Конечная цель гормонотерапии — не допустить поступления половых гормонов в раковую клетку молочной железы, чем нарушается синтез необходимых для её жизни веществ и вынужденно включается программа клеточной гибели — апоптоз.
В качестве гормональных (эндокринных) лекарственных средств при раке молочной железы используют:
- натуральные гормоны и их синтетические аналоги — эстрогены, андрогены и прогестины;
- блокирующие связывание естественного гормона с рецептором опухолевой клетки антигормоны — антиэстрогены;
- нарушающие локальный синтез гормонов в жировой ткани ингибиторы ароматазы;
- гонадотропин-релизинг-гормон — химическое вещество, подменяющее естественный гормон гипоталамуса, который блокирует синтез яичниками собственных половых гормонов.
Аналогично гонадотропин-релизинг-гормону действуют хирургическое удаление придатков или облучение яичников, без них невозможно лечение менструирующих женщин ингибиторами ароматазы.
Показания для назначения
Рак молочной железы возникает на фоне гормонального дисбаланса, но не все опухоли чувствительны к гормональному воздействию, некоторые популяции клеток не используют половые гормоны для своей жизнедеятельности — они гормонально независимы. Как правило, независимой считается опухоль, в которой не больше 1% клеток нуждается в эстрогенах.
О гормональной зависимости злокачественного новообразования молочной железы судят по наличию на ядерных мембранах клеток рака специальных гормональных рецепторов, взаимодействующих с эстрогенами и переносящих их внутрь клеточного ядра, кратко обозначаемых как «ЭР+» или «ER+». Рецепторы определяет специальный анализ.
Дополнительный косвенный признак гормонозависимого рака молочной железы — наличие мембранных рецепторов прогестерона — «ПР+» или «PR+», пороговое значение — более 20% клеток в популяции.
Наиболее благоприятно для назначения гормонотерапии при раке молочной железы сочетание максимально высокого уровня ЭР+ с ПР+. Формально гормонотерапия показана всем пациенткам, в опухоли молочной железы которых имеется более 1% клеток ЭР+ без учёта концентрации ПР+.
Особенности гормонотерапии при раке молочной железы
Гормональная зависимость рака молочной железы обещает чувствительность к гормонотерапии, но не гарантирует её.
Во-первых, не все ЭР способны взаимодействовать с лекарственным препаратом, нацеленным на него антиэстрогеном. Результат лечения прогнозирую по объёму популяции чувствительных клеток, считается, что чем больше в раке ЭР+, тем эффективнее будет эндокринная терапия.
Во-вторых, некоторые опухоли формируют устойчивость к лекарству, ускоренно разрушая его в своей цитоплазме или выводя из клетки в межклеточную жидкость. Формирование устойчивости легло в основу поэтапной гормонотерапии, когда при утрате опухолью чувствительности к одному препарату переходят на другую группу лекарственных средств. Особенность рака молочной железы — возможность перехода с одной линии гормонотерапии на другую при снижении клинической эффективности воздействия.
В-третьих, ради собственного выживания на фоне гормонотерапии опухоль постепенно становится нечувствительной к препарату, происходит естественный отбор — реагирующие на гормональные лекарства клетки погибают, выживают и дают потомство нечувствительные. Отчасти на этой особенности рака молочной железы базируется отказ от одновременного использования химиотерапии и гормонотерапии — только последовательно.
И третья особенность — при подборе лекарственного препарата обязательно учитывается гормональный период, в котором пребывает женщина, при недавнем прекращении менструации определяется концентрация производимых гипофизом лютеинезирующего (ЛГ) и фолликулостимулирующего (ФСГ) гормонов, стимулирующих работу яичников.
Виды гормональной терапии
В зависимости от цели гормонотерапию подразделяют на неоадъювантную, адъювантную и лечебную.
Неоадъювантная ГТ проводится до радикальной операции для уменьшения объема опухолевого узла и уничтожения микрометастазов, попутно выясняется клиническая чувствительность опухоли к конкретному лекарственному препарату и перспективность профилактической антигормональной терапии после операции. Этот вид ГТ назначается при люминальном молекулярно-биологическом подтипе рака молочной железы с ЭР+ и ПР+. Эффект при гормонотерапии отсроченный, в отличии от химиотерапии, поэтому неоадъювантное лечение проводится не менее 4 месяцев, при хорошем результате — 8 месяцев и дольше, соответственно, на такой же срок откладывается операция на молочной железе. Поскольку наименее токсичными считаются ингибиторы ароматазы, их и используют, но они разрешены только для переживших менопаузу женщин.

Адъювантная гормонотерапия назначается для профилактики рецидива и метастазирования, она проводится всем больным с ЭР+, в том числе при карциноме in situ, только цель при 0 стадии иная — предотвращение развития рака в другой молочной железе. Продолжительность терапии — до прогрессирования или 5-10 лет в зависимости от исходного прогноза, а начинают ГТ строго после завершения адъювантной химиотерапии. Выбор препарата зависит от менструального статуса женщины.
Лечебная ГТ применяется при неоперабельном раке молочной железы или метастазах после радикального лечения. Длительность эндокринного воздействия зависит от эффективности, при прогрессировании переходят на следующий по очереди лекарственный препарат, выбор которого определяется по гормональному статусу женщины.
Препараты
Гормональная терапия рака молочной железы проводится антиэстрогенами и ингибиторами ароматазы, применение эстрогенов, прогестинов и андрогенов ограничено высокой частотой осложнений. Каждый препарат в лечебных целях принимают до прогрессирования заболевания, в профилактически — до появления метастазов или не менее 5 лет.
Антиэстрогены представлены двумя препаратами:
- ежедневно принимаемые при всех видах ГТ и в любом гормональном периоде таблетки тамоксифена;
- фулвестрант (Фазлодекс™) используется при распространенном раке молочной железы, ранее прогрессировавшем на тамоксифене, и только после менопаузы, он вводится в мышцу раз в месяц, главный недостаток — стоимость инъекции около 500$.
Ингибиторы ароматазы в таблетках для ежедневного приема применяются при любом виде ГТ у женщин после менопаузы, все лекарства одинаково эффективны:
- анастрозол (Аримидекс™);
- летрозол (Фемара™);
- эксеместан (Аромазин™).
Никогда одновременно не используются лекарственные средства разных групп — только по-отдельности. Некоторые схемы адъювантной ГТ предполагают смену лекарства через определенный срок, например, молодая женщина 5 лет пьет тамоксифен, при прекращении менструальной функции ещё 2 года получает ингибиторы ароматазы. При лечении неоперабельного рака или метастазов смена группы происходит при возобновлении опухолевого роста или появлении выраженных побочных осложнений.
Для временного выключения функции яичников у менструирующих женщин применяются аналоги гонадотропин-рилизинг-гормона (ГРГ), при раке молочной железы Стандарты рекомендуют каждые 28 дней инъекцию одного из одинаково эффективных средств:
- гозерелин (Золадекс™);
- трипторелин (Диферелин™);
- бусерелин (Бусерелин-депо™);
- лейпрорелин (Люкрин-депо™)
Группа ГРГ вспомогательная, используется вместе с ингибиторами ароматазы или антиэстрогенами. Прием таблеток начинают после полутора-двух месяцев инъекций антагонистов гонадотропинов. ГРГ конкуренты удаления или облучения яичников, после прекращения инъекций менструация у молодых женщин восстанавливается в ближайшие 3 месяца.
Побочные действия
Антиэстрогены и ингибиторы ароматазы обладают схожими побочными реакциями, самые опасные из которых: образование тромбов и дисгормональный остеопороз. Тамоксифен активнее влияет на свертываемость крови, и при многолетнем использовании у небольшого процента женщин индуцирует рак эндометрия. Ингибиторы ароматазы чаще осложняются остеопорозом. Одинаково часто обе группы вызывают приливы.
Все гормональные препараты подвергаются трансформации в печени. Тамоксифен может вызвать токсическое поражение печени и привести к застою желчи — холестазу, клиника которого отчасти напоминает острый холецистит, все симптомы исчезают после отмены антиэстрогена.
В настоящее время нет однозначного мнения по выбору лекарственного средства — эффективность их одинаковая, поэтому ориентируются на гормональный возраст и сопутствующую патологию, к примеру, при варикозной болезни или патологии эндометрия целесообразно избегать тамоксифена, при остеопорозе — ингибиторов.
В подавляющем большинстве случаев ГТ хорошо переносится, что позволяет при неблагоприятных прогностических факторах пролонгировать её до 7-10 лет.
Возможные последствия
На фоне приёма тамоксифена:
- при метастазах в костях рака молочной железы в первый месяц лечения могут усилиться боли — синдром «вспышки» требует отмены антиэстрогена;
- стимулируется овуляция и возможна беременность, поэтому женщины репродуктивного возраста должны прибегать к контрацепции;
- течение кардиальных заболеваний улучшается вследствии благоприятного действия на обмен липидов, но только после нескольких лет ГТ;
- опосредованное повышение в крови эстрогенов приводит к приливам, но также несколько «омолаживает» кожу и слизистые половых органов;
- осложнения со стороны глаз редки, но возможно обострение давней ретинопатии, кератопатии или усугубление возрастной катаракты.
Использование препарата группы ГРГ часто сопровождается посткастрационным синдромом с приливами, частыми кольпитами, недержанием мочи, болями в мочевом пузыре и т.д. У женщин в пременопаузе при совместном применении ГРГ с ингибитором ароматазы возможно повышение уровня эстрадиола, что исключает эффект от лечения.
Диета при гормонотерапии
Многие женщины считают, что на фоне гормональных препаратов растет вес тела, клинические исследования на счет ГТ относят всего лишь 1,6% — 4% случаев повышения веса. Избыток веса обусловливается не фармакологическим действием, а изменением ритма жизни после выявления рака молочной железы, нормализацией питания после завершения химиотерапии и снижением уровня стресса после проведения радикальной терапии. На профилактической ГТ женщина успокаивается и бережет себя, избегая физических нагрузок, и вес растет даже без лекарств.
Гормонотерапия не нуждается в особой диете, необходима коррекция питания с учетом ежедневных нагрузок и сопутствующих болезней.
Эффективность
Результат терапии зависит от чувствительности опухолевых клеток к лекарствам, поэтому в обязательном порядке до начала лечения определяется молекулярно-биологический подтип рака молочной железы.
Эффект адъювантной терапии оценивается по времени появления метастазов — на фоне ГТ или в течение года после её завершения. В отсутствии клинически определяемой опухоли косвенно об эффективности свидетельствует уровень эстрадиола в крови.
Результат гормонального воздействия более медленный, нежели химиотерапии, поэтому оценка эффективности при распространенном раке молочной железы проводится каждые 3-4 месяца приема. Общий эффект ГТ — от 15% до 36%, и тем выше, чем больше концентрация ЭР и ПР.
Прогноз при применении гормонотерапии
Распространенность рака молочной железы на момент выявления косвенно свидетельствует об агрессивности и гормональной независимости опухоли. ГТ мало полезна при метастатической стадии, сопровождающейся висцеральным кризом — при множественных злокачественных новообразованиях внутренних органов с нарушением их функции.
При распространенном процессе с высоким уровнем ЭР и ПР на фоне ГТ регрессируют множественные метастазы, особенно в костях, коже и лимфоузлах, даря женщине годы качественной жизни. Эндокринное воздействие бесполезно при прогрессировании рака молочной железы на фоне трех линий ГТ.
Лечение рака должно быть своевременным и адекватным, в нашей Клинике проводится геномный анализ опухоли на чувствительность к лекарствам, что повышает непосредственные результаты терапии и сказывается на продолжительности жизни больных.
Список литературы:
- Стенина М.Б., Жукова Л.Г., Королева И.А., Пароконная А.А., Семиглазова Т.Ю., Тюляндин С.А., Фролова М.А. Практические рекомендации по лекарственному лечению инвазивного рака молочной железы. Злокачественные опухоли. — 2016. — № 4. Спецвыпуск 2.
- Davies C., Pan H., Godwin J. et al. /Long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of oestrogen receptor-positive breast cancer: ATLAS, a randomized trial// Lancet 2013; 381.
- Dowsett M./ Neoadjuvant endocrine therapy: patient selection, treatment duration and surrogate endpoints// Breast 2015; 24(Suppl 1)
- Hart C.D., Di Leo A./ Defining optimal duration and predicting benefit from chemotherapy in patients with luminal-like subtypes// Breast 2015; 24(Suppl 1):
- Francis P.A., Regan M.M., Fleming G..F et al. /Adjuvant ovarian suppression in premenopausal breast cancer// N Engl J Med 2015; 372
- Pagani O., Regan M.M., Walley B.A. et al. /Adjuvant exemestane with ovarian suppression in premenopausal breast cancer// N Engl J Med 2014; 371: 107–118.
- Regan M./ Predicting benefit of endocrine therapy// Breast 2015; 24(Suppl 1).
Источник